推荐产品
公司新闻/正文
细胞分选与癌症免疫治疗:来自同行的经验分享
人阅读 发布时间:2019-03-13 17:34

免疫疗法如今在众多癌症治疗方法中占据着最有前景的地位。来自美国Fred Hutchinson癌症研究中心和Providence癌症研究所从事免疫治疗的研究人员分享了他们从事免疫疗法项目中的一些经验和方法。
Dr. Eric Tran就职于俄勒冈州波特兰市的Providence癌症研究所的Earle A. Chiles Research Institute,他专注于癌症的过继性细胞疗法(adoptive cell therapy)研究。他强调说,"数十年来治疗癌症的最主要方法都是手术、放疗及化疗。不过这些形式的手段只对局部及早期癌症有效,而无法治愈患有恶性癌症(尤其实体组织癌症)的病人,鲜有例外。而如今已证实免疫疗法可以带来持续性作用,时常可以治愈采取其他手段无法治愈的病例。"。过继性细胞疗法(adoptive cell therapy)或过继性免疫疗法(adoptive immunotherapy),是一种利用病人自体免疫系统对抗癌症的新型治疗手段。
利用T细胞反应抵御癌症非常有效,因为这些细胞可以被精确地、高度特异性地导入至癌症位点,并且有记忆效应可以持续发挥作用。
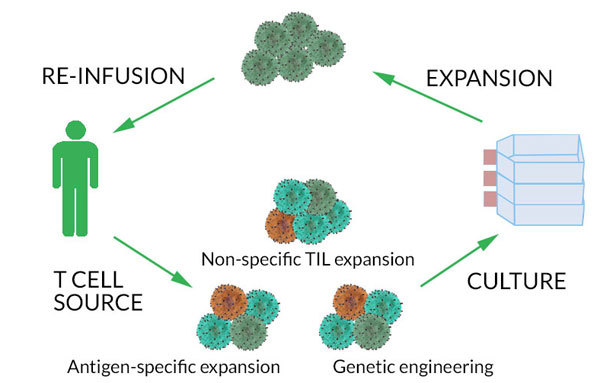
过继性T细胞免疫疗法需要将癌症反应性T细胞扩增培养然后回输至病人体内。所示的肿瘤浸润淋巴细胞(TILs)含有肿瘤特异性的T细胞,而通常外周血中的淋巴细胞中癌症反应性的T细胞比例很低,需要预先富集。
Dr. Tran受训于领域先驱Dr. Steven Rosenberg实验室,如今正活跃于过继性细胞疗法研究领域的的最前沿。Dr. Tran实验室专注于鉴定肿瘤反应性的T细胞并将其扩增用于回输至病人体内,以期这些细胞将归巢于肿瘤部位从而介导消灭肿瘤。
用于过继性免疫疗法的T细胞可以从病人血液或是实体瘤中分离得到,经过扩增培养然后回输至病人体内。不同于血液中T细胞比例较低,来自肿瘤的T细胞(即肿瘤浸润的免疫细胞,TILs)通常在肿瘤部位较为富集。这种过继性移植手段已被用于治疗较难治愈的疾病如恶性黑色素瘤(Ref.1-5)。
在西雅图Fred Hutchinson癌症研究中心,正在进行的免疫疗法临床试验主要集中在梅克尔细胞癌、急性髓系白血病和急性淋系白血病。其流式细胞学中心实验室主任Andrew Berger表示,“我们也在尝试将细胞分选用于过继性治疗应用——这是种永久性持续起作用反应,因此不再有复发风险。”

西雅图Fred Hutchinson癌症研究中心(图片来自网络)
“大多数癌症患者体内存在一些可以特异性识别癌症的T细胞。部分T细胞可以识别一种我们称之为新抗原(neoantigen),这种抗原由癌症中突变的基因所编码。”Dr. Tran解释说,“我们应用了一种生物信息学手段来鉴定这些癌症突变并测试每个患者体内的T细胞是否可以识别其独特的新抗原组。”Dr. Tran实验室的研究目标是鉴定每个患者体内识别新抗原的T细胞并将其用作免疫疗法。
高纯度标准无可商榷
应用TILs进行免疫疗法的关键步骤在于肿瘤反应性T细胞的回输。但用于回输的细胞产品可能含有高比例的非肿瘤反应性T细胞,当被回输到病人体内后这部分细胞会因为与肿瘤反应性T细胞竞争生长因子而阻碍免疫疗法的发挥作用。因此将癌症反应性T细胞从非反应性T细胞中鉴定、筛选和分离出来是必不可少的工作。一种办法就是利用流式分选仪对目的细胞进行分离纯化。研究人员和临床医生利用流式细胞技术可以对T细胞同时进行鉴定和分选工作。
Dr. Tran说“在此阶段我们需要的是高纯度的肿瘤反应性T细胞。例如在共培养条件下,很多时候肿瘤反应性T细胞的比例非常低。比如只有1%的细胞群体具有肿瘤反应效应,我们需要将这些细胞分离至高纯度以确保没有非反应性T细胞的污染。”
对于Fred Hutchinson的临床方案,情况与上述类似。Berger表示“得率很重要,但纯度更重要。针对要回输的细胞我们有特定的标准,比如说80%。我们观察到,当细胞被扩增之后如果目标细胞群体纯度低于98%则另外2%的细胞可能会超过目标细胞群的生长速度,因此我们只能再作一次分选之后才能回输给患者。”
Providence癌症研究所和Fred Hutchinson癌症研究中心均采用了Sony FX500细胞分选仪 进行细胞治疗项目的细胞分选工作。
“将细胞分选仪用于治疗患者时的首要因素是纯度和无菌。同时仪器也应当尺寸紧凑和操作方便,以便于在洁净室环境下使用。”流式细胞中心实验室的管理员Miranda Gilchrist表示,这家中心实验室负责为Providence癌症研究所的数十个免疫治疗项目提供技术服务,其中也包括Dr. Tran实验室。
Gilchrist表示,“Sony FX500细胞分选仪从样本上样针到芯片均为可一次性更换式液路。我们可以为每位患者更换仪器的全部液路,所有液路均经过放射灭菌处理。这对患者的安全至关重要,是我们选择Sony FX500的主要考虑。”

位于俄勒冈州的Providence癌症研究所(图片来自网络)
简便易用的手段不可忽视
操作方便对从事细胞治疗项目的科学家来说非常关键,迫不得已而依赖于个别仪器操作人员来进行肿瘤特异性T细胞的分选工作,对他们来说变得越来越难以接受。例如Fred Hutchinson流式细胞中心实验室如今为4项基于过继免疫疗法的临床试验以及大量科研用户提供服务。轻松的培训工作对于让具有不同研究背景的科学家能够满怀信心地进行细胞分选工作来说至关重要。Berger说道,“我们的仪器服务于大约450家客户,因此我们需要做大量的培训工作。”

Sony FX500全液路可更换式细胞分选仪
“我们主要是培训客户如何正确操作仪器及如何进行数据分析。因此对我们来说,我们优先考虑便于对用户进行培训的仪器平台。操作方便也是一个重要的考量因素。”Berger说,“我们中心实验室会有很多各种不同研究背景的人来使用仪器。我们很早之前就跟索尼公司提及我们旧有细胞分选系统的各种局限。旧系统因为需要专业知识才可操作,因此扩展性较差,在旧系统上我们每周完成不了几次分选实验。”
Fred Hutchinson的中心实验室近期新添置了一台Sony FX500细胞分选仪。“我们可以对所有员工培训这台仪器——我们已经培训了十六七位。这台仪器安装一次性部件只需要大约20分钟,而且全部可由向导软件指导完成。”Berger补充道,“我们(平台操作人员)仍然可以以流式专家身份(为用户提供支持),但有一台方便操作的仪器是件很棒的事情,因为你无需依赖专家就可完成治疗性细胞分选。便于操作、容易培训,这使得索尼FX500能够在同类产品中脱颖而出。”
展望未来
“当前的免疫治疗领域是非常令人振奋的。我从事这方面工作已经相当长时间了,亲眼目睹了研究项目从纯研究的水平发展到可以带来直接的临床价值”,Berger说,“每年有很多新的临床试验上马。这些新型的过继免疫疗法对人体毒性小,所以的确能带来很大不同。”
大部分基于免疫疗法的临床试验招募的都是晚期癌症病人。过继性T细胞免疫疗法的一个潜在好处是可以被应用于处于疾病早期的病人,从而完全摆脱对化疗或放疗的需求。
科研实验室里的过继免疫疗法项目面临的挑战是如何把项目扩展到临床水平。如同Dr. Tran指出的那样:“不同于化疗或其他药物的现成方案,细胞治疗产品的生产技术复杂度高,且对每个病人都是个性化的。如果这些手段被证实能够有效治疗最为棘手的癌症,那么为实施治疗和简化过程的基础设施及操作方法肯定也必定会得到长足发展。”
下一步……
在这些研究实验中仍有许多困难需要克服,Dr. Tran继续说道,“我们希望对癌症反应性的T细胞的生物学特征有更深入的理解。为了提升病人对免疫治疗的响应,我们必须更加深入的了解癌症及免疫系统。”众所周知,癌症利用多种分子机制来逃避免疫系统反应,因此使得很多为免疫治疗所做的努力徒劳无功。Dr. Tran总结说,“癌症能自身发展出免疫抵抗力。搞清楚癌症是如何逃避免疫系统的反应、以及我们应如何优化治疗方法来真正克服其免疫抵抗的机制,将是免疫治疗领域发展的下一个助推力量。”
(编译自SelectScience网站)
Reference
1. Brentjens RJ, Davila ML, Riviere I, et al. CD19-targeted T cells rapidly induce molecular remissions in adults with chemotherapy-refractory acute lymphoblastic leukemia. Science Transl Med. 2013;5:177.
2. Maude SL, Frey N, Shaw PA, et al. Chimeric antigen receptor T cells for sustained remissions in leukemia. N Engl J Med. 2014;371:1507-1517.
3. Turtle CJ, Hanafi L-A, Berger C, et al. Immunotherapy of non-Hodgkin’s lymphoma with a defined ratio of CD8+ and CD4+ CD19-specific chimeric antigenreceptor–modified T cells. Science Transl Med. 2016;8:355RA116.
4. Rosenberg SA, Packard BS, Aebersold PM, et al. Use of tumor-infiltrating lymphocytes and interleukin-2 in the immunotherapy of patients with metastatic melanoma. N Engl J Med. 1988;319:1676-1680.
5. Robbins PF, Lu YC, El-Gamil M, et al. Mining exomic sequencing data to identify mutated antigens recognized by adoptively transferred tumor-reactive T cells. Nat Med. 2013;19:747-752.









